このページでは2018年度の岡山県立入試一般選抜(前期)の問題を解説しています。(理科のみ)
問題・模範解答はこちら↓↓↓↓
https://resemom.jp/feature/public-highschool-exam/okayama/2018/science/i_question01.html
大問1の解説
①
図2のXY部分にあるのは寒冷前線です。
寒冷前線では
寒気が暖気を押し上げるように進んでいきます。
つまりウのような断面です。
一方で温暖前線では
暖気が寒気をはい上がるように進んでいきます。
つまりイのような断面です。
寒気は暖気よりも重い(密度が高い)ため、基本的に寒気が下に、暖気が上に来ます。
②
空気中に水蒸気が入りきらなくなった時、入りきらなかった分が水滴へと変化します。
まず含まれている水蒸気量は次の式で求められます。
$$実際の水蒸気量=飽和水蒸気量×\frac{湿度}{100}$$
※湿度の公式を変形したものです。
この問いでは、「15℃・湿度75%の空気」を考えているので
$$実際の水蒸気量=12.8×\frac{75}{100}=9.6g$$
温度を5℃まで下げているので
$$入りきらなくなる水蒸気=9.6-6.8=2.8g$$
となります。
よって2.8gが答えです。
POINT!!
水滴の量を求めるには
空気中に入らなくなった水蒸気の量を求めればよい。
③
霧は前問②のように、入りきらなくなった水蒸気が水滴になったことで生じるものです。
(霧はごく小さな水滴の集まり)
たくさん水滴ができる(=霧ができやすい)のは
・空気中に水蒸気がたくさん含まれている=湿度が高い
・温度が大きく下がる=昼夜の気温差が大きい
ときです。
⑤
金属の共通の性質には
・電気を通しやすい。
・熱を通しやすい。
・みがくと光沢が出る。
・たたくとうすく広がる、のびる。
というものがあります。
磁石に引き寄せられるかどうか、は金属共通の性質ではありません。
むしろ磁石に引き寄せられる金属は少なく、鉄・ニッケルなどです。
POINT!!
磁石に引き寄せられる金属は、鉄・ニッケルなどのごく一部だけ!
⑥
図3のような電池では、各金属板でどのようなことが起こっているかを押さえておきましょう。
亜鉛板では・・・
亜鉛板が液中に溶けだし、電子を失って亜鉛イオンZn2+になっている。
銅板では・・・
液中の水素イオンが近づいて、電子を得て水素原子Hになっている。
その水素原子が2個集まり気体の水素H2として発生。
銅板が+極、亜鉛板が-極になっています。
⑦
動物細胞・植物細胞の共通なつくりは
核・細胞質・細胞膜
の3つ。
植物細胞にのみ見られるつくりは
細胞壁・液胞・葉緑体
の3つ。
⑧(1)
凸レンズ1枚を通して実像を見たとき、
その実像はもとの物体と上下左右が逆向きに見えます。
⑧(2)
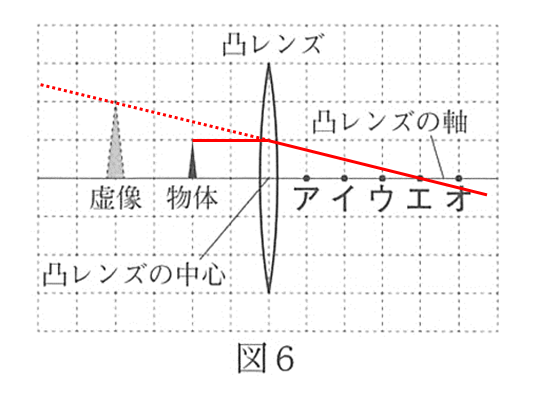
凸レンズの作図方法を覚えておきましょう。
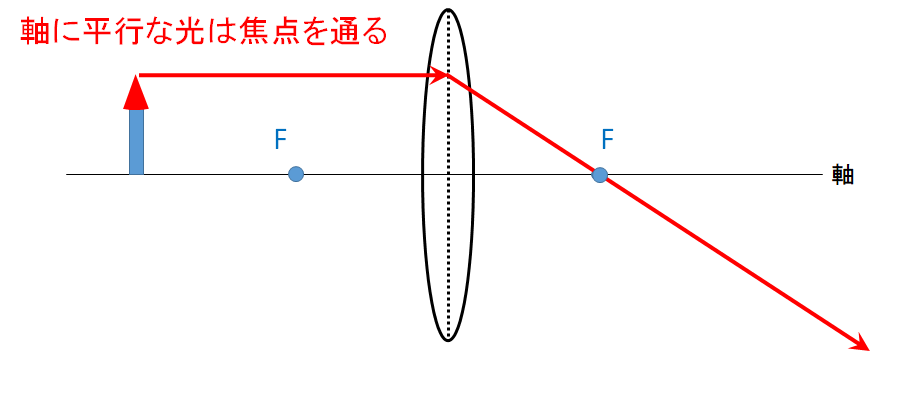
▼軸に平行にやってきた光・・・焦点を通る
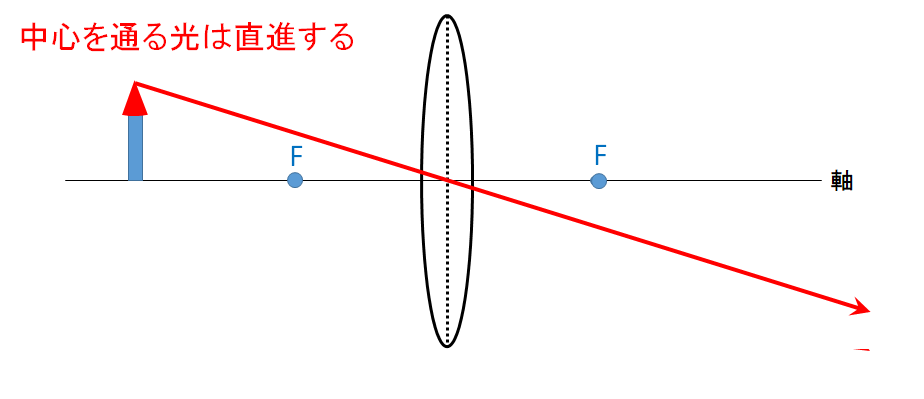
▼レンズの中心を通る光・・・そのまま直進
▼焦点を通ってやってきた光・・・軸に平行に進む
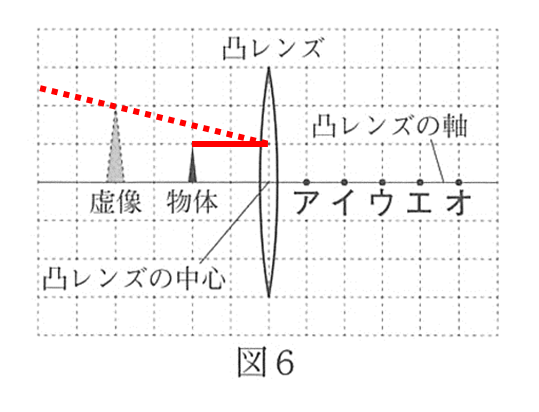
図6の場合、まず軸に平行な光を作図しましょう。(↓の図)
これは焦点を通るはず。
しかし今は焦点の位置がわかっていません。
ですが虚像の位置がわかっているので、↓のような作図で虚像の位置を求めているはず。
これを右下に延長してみます。(↓の図)
よってエが焦点であるとわかります。
大問2の解説
①(1)
ツユクサ・・・被子植物の単子葉類
マツ・・・・・裸子植物
アブラナ・・・被子植物の双子葉類
ゼンマイ・・・シダ植物
ソテツ・・・・裸子植物
③
地点Aの水質階級を求めましょう。
○や●がついているのはカワゲラ・ヒラタドロムシ・カワニナ・シマイシビルです。
カワゲラは○、水質階級Ⅰの生物 → 水質階級Ⅰが+1点
ヒラタドロムシは●、水質階級Ⅱの生物 → 水質階級Ⅱが+2点
カワニナは●、水質階級Ⅱの生物 → 水質階級Ⅱが+2点
シマイシビルは○、水質階級Ⅲの生物 → 水質階級Ⅲが+1点
よって地点Aの点数は
階級Ⅰ・・・1点
階級Ⅱ・・・4点
階級Ⅲ・・・1点
階級Ⅳ・・・0点
水質階級はもっとも高い点数の階級で決まります。
つまり地点Aの水質階級はⅡにあたるということです。
同じようにB地点の点数を求めると
階級Ⅰ・・・0点
階級Ⅱ・・・2点
階級Ⅲ・・・3点
階級Ⅳ・・・1点
したがって地点Bの水質階級はⅢです。
同様にしてC地点の点数は
階級Ⅰ・・・4点
階級Ⅱ・・・3点
階級Ⅲ・・・0点
階級Ⅳ・・・1点
したがって地点Cの水質階級はⅠです。
以上から、地点A~Cを汚い順に並べると
B→A→Cとなります。
大問3の解説
②
実験1の結果からCはアルカリ性とわかります。
よってCは水酸化バリウム水溶液です。
実験2の結果からDは酸性であるとわかります。
よってDは硫酸です。
ここまででA・Bは食塩水・砂糖水のいずれかとわかります。
実験3で、Aは電気を通さないため、砂糖水であるとわかります。
したがってBは食塩水となります。
③
強い酸は金属と反応して水素を発生します。
※強い酸・・・硫酸・塩酸・硝酸など。炭酸や酢酸は弱い酸。
④(2)
この実験では、「水酸化ナトリウム水溶液の入ったビーカー」に塩酸を加えています。
実験のはじめは、ビーカーには水酸化ナトリウム水溶液が入っているだけ。
すなわち水素イオンは存在しません。
よってこの時点で正解はイ・ウのどちらかに絞られます。
塩酸を加えるにつれて、中和反応が起こります。
塩酸の水素イオンは中和反応に使われ、水へと変化します。
つまり、しばらくの間、水素イオンは増えないのです。
したがってそのような変化をしているのはウのみです。
大問4の解説
①(2)
黒点はまわりよりも温度が低いところ。
太陽を観察していると黒点の位置が移り変わっていきます。
これは太陽が自転している証です。
また太陽の黒点は中央にあるときは丸く、ふちにきたときは細く見えます。
これは太陽が球形をしている証です。
③(2)
(1)からGは地球型惑星であることがわかります。
地球型惑星は、水星・金星・地球・火星の4つ。
表から、惑星Gの太陽からの平均距離は1.52とあるため、惑星Gは地球よりも外側にある惑星ということになります。
よって惑星Gは火星であると考えられます。
大問5の解説
④
表1のⅡの結果から、オームの法則を用いて
$$抵抗=\frac{電圧}{電流}=\frac{3V}{0.2A}=15Ω$$
よって15Ωが正解とわかります。
⑤
電力・電流・電圧は次の式のような関係があります。
$$電力(W)=電流(A)×電圧(V)$$
100Vの電圧でドライヤーを使ったとき、電力は1100Wなので
$$電流=\frac{電力}{電圧}=\frac{1100W}{100V}=11A$$
100Vの電圧でテレビを使ったとき、電力は210Wなので
$$電流=\frac{電力}{電圧}=\frac{210W}{100V}=2.1A$$
100Vの電圧でこたつを使ったとき、電力は600Wなので
$$電流=\frac{電力}{電圧}=\frac{600W}{100V}=6A$$
100Vの電圧で掃除機を使ったとき、電力は1200Wなので
$$電流=\frac{電力}{電圧}=\frac{1200W}{100V}=12A$$
100Vの電圧でパソコンを使ったとき、電力は100Wなので
$$電流=\frac{電力}{電圧}=\frac{100W}{100V}=1A$$
例えばアのようにドライヤーとこたつを同時に使うと
$$11A+6A=17A$$
の電流が流れます。
許容電流15Aを超えてしまっているので、アは不適切です。
イの場合は、掃除機とテレビを同時に使っているため
$$12A+2.1A=14.1A$$
の電流が流れます。
許容電流15Aを超えていないため、イは適切です。
同様にウ・エ・オの場合の電流も求めるとイ・エのみが適切(許容電流を下回る)とわかります。




コメント(承認された場合のみ表示されます)