1.発熱反応と吸熱反応
■発熱反応
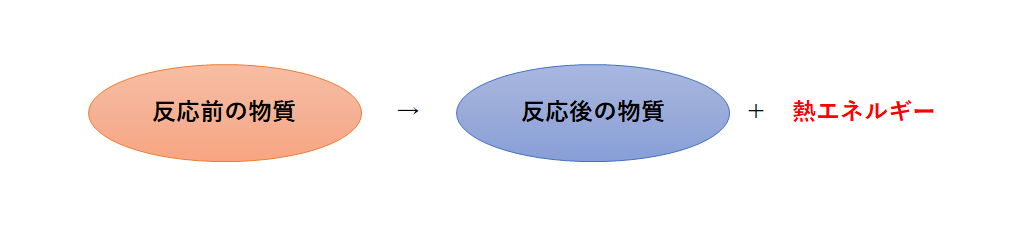
反応後に熱が発生する化学変化のこと。
反応後に温度が上がっている。
■吸熱反応
反応前に熱が吸収される化学変化のこと。
反応後に温度が下がっている。
■エネルギーについて
※化学エネルギー・・・物質がもつエネルギーのこと。
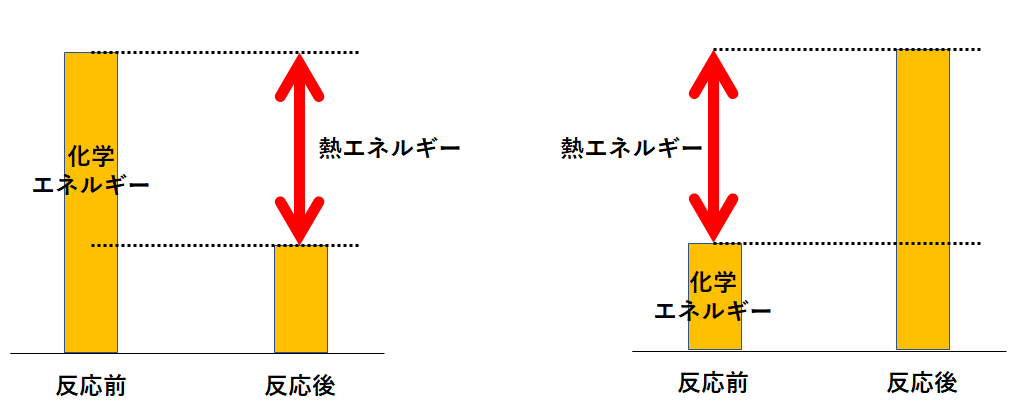
左の図が発熱反応のイメージ、右の図が吸熱反応のイメージです。
化学変化は主に発熱反応または吸熱反応に分かれます。
しかしそれらすべてを覚えることは難しいのでよく出題されるものだけを覚えておきましょう。
よく出題される発熱反応
・燃焼
熱や光をともなう酸化のこと。(→【酸化と燃焼】←で解説中)
・中和反応
酸とアルカリの反応のこと。(中3で学習。→【中和反応】←で解説中)
・鉄+硫黄→硫化鉄
鉄と硫黄の化合のこと。(→【化合】←で解説中)
化学反応式では Fe + S → FeS と書く。
・鉄+酸素→酸化鉄
鉄の酸化のこと。
・酸化カルシウム+水→水酸化カルシウム
少しマニアック。
化学反応式では CaO + H2O → Ca(OH)2 と書く。
よく出題される吸熱反応
・塩化アンモニウム+水酸化カルシウム→アンモニア
中1で学習したアンモニアの代表的な発生方法。(→【気体の性質】←で解説中)
化学反応式では 2NH4Cl + Ca(OH)2 → 2NH3 + CaCl2 + 2H2O と書く。
・クエン酸+炭酸水素ナトリウム→二酸化炭素
※「~アンモニウム」がからむ反応・「クエン酸」がからむ反応は吸熱反応です!
2.化学かいろ
化学かいろは寒い日に使うあれです。
袋から取り出してしばらくするとあたたかくなる道具です。
その中身は
・鉄粉・・・・・酸素と化合して熱を発生させる
・活性炭・・・・酸素を集まりやすくしている
・食塩(水)・・・酸化の速度をはやめている
となっています。
鉄の酸化が発熱反応であることを利用した道具と言えます。
そんなに出題はされませんが余裕があれば覚えておきましょう。


コメント(承認された場合のみ表示されます)
[…] https://chuugakurika.com/2017/12/29/post-1231/ […]