このページでは「炭酸水素ナトリウムの熱分解」「酸化銀の熱分解」「水の電気分解」について解説しています。
「熱分解」の動画による解説は↓↓↓
「水の電気分解」の動画による解説は↓↓
1.分解
■分解
化学変化の1つ。
1種類の物質が2種類以上の物質に変化すること。
■熱分解
加熱をすることで分解すること。
■電気分解
電圧を加えることで分解すること。
2.熱分解
(例)炭酸水素ナトリウムの熱分解
(反応の様子) 炭酸水素ナトリウム → 炭酸ナトリウム + 水 + 二酸化炭素
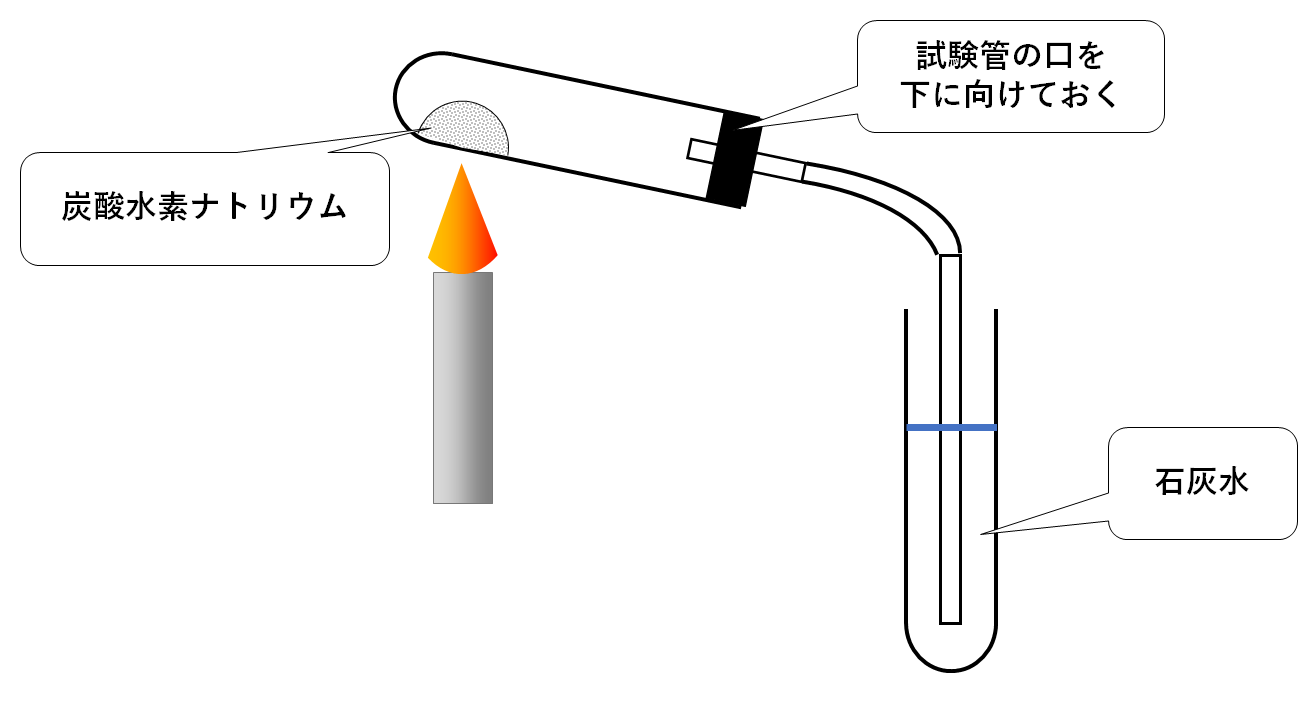
炭酸水素ナトリウムの粉末(白色)を試験管に入れて加熱すると、水と二酸化炭素が発生し、試験管には炭酸ナトリウムの固体(白色)が残ります。
・二酸化炭素は石灰水を白くにごらせます。
・水は塩化コバルト紙を青色から赤色に変化させます。
・炭酸水素ナトリウム・炭酸ナトリウムともに白色で見分けがつきにくい物質です。しかし、わずかに違いがあります。
・炭酸水素ナトリウムは重そうやふくらし粉、ベーキングパウダーに使われています。
※パンにはふくらし粉が使われていますが、パンを加熱することで二酸化炭素が発生し、パン生地を押し上げるためです。
この実験では重要な注意点があるので覚えておきましょう。
・試験管の口を下げておく。
→ 発生した液体が加熱部分に流れ、試験管が割れるのをふせぐため。
・火を消す前に、石灰水からガラス管を抜いておく。
→ 石灰水が逆流して、試験管が割れるのをふせぐため。
(例2)酸化銀の熱分解
(反応の様子) 酸化銀 → 銀 + 酸素
試験管内で酸化銀(黒色)を加熱すると、試験管には銀(白色)が残り、酸素が発生します。
・発生した気体が酸素かどうか確かめるには、火のついた線香を近づけて激しく燃えるかを確認します。
・酸素は、水に溶けにくいため水上置換法で集めます。
3.電気分解
(例)水の電気分解
(反応の様子) 水 → 水素(陰極) + 酸素(陽極)
↑の図のような「H字管」という装置を使います。
または「簡易電気分解装置」を使って実験することも多いです。
このような電気分解のための装置には
電源装置の+極側につながった電極=陽極
電源装置のー極側につながった電極=陰極
があります。
・陰極側には水素が発生します。発生した気体が水素かどうか確かめるには、火のついたマッチを近づけて音を立てて燃えるかを確認します。
・陽極側には酸素が発生します。発生した気体が酸素かどうか確かめるには、火のついた線香を近づけて激しく燃えるかを確認します。
・発生する体積比は、水素:酸素=2:1です。
・水は電気を通しにくいです。水酸化ナトリウム(または硫酸)を溶かして電気を通しやすくします。
※そのため「水の電気分解」ではなく「水酸化ナトリウム水溶液の電気分解」と表記されることもあります。
・図のようなH字管を用いる場合、ピンチコックを開けてその下のビーカーに水が少しずつ滴下するようにしておきます。
⇒ 気体がたまってゴム栓が飛んで行ってしまうのをふせぐためです。
・水酸化ナトリウムの量は変化せず、水のみ(水素と酸素に変化するため)減少します。よって水溶液としての濃度は上がります。
(例2)塩化銅水溶液の電気分解
(反応の様子) 塩化銅 → 銅(陰極) + 塩素(陽極)
・塩化銅水溶液は青色をしています。
・反応が進むと青色がうすくなります。
・銅は赤色(赤褐色)の金属です。
・塩素は以下の①~⑤のようなさまざまな性質を持ちます。
①プールの消毒のにおいがする。(刺激臭と呼ぶこともある)
②水に溶けやすいので,集めにくい。
③黄緑色の気体。
④脱色・漂白作用がある。⇒赤インクなどを近づけると無色になる。
⑤有毒な気体で殺菌作用がある。
電気分解の詳しい原理は
→【塩酸の電気分解】←
→【塩化銅水溶液の電気分解】←
→【*水の電気分解】←
で解説中。
中3で学習する内容です。
POINT!!
・炭酸水素ナトリウムの熱分解と水の電気分解が特によく出題される。
・「何が生じるか」だけでなく、塩化コバルト紙や石灰水の反応、体積比、陽極と陰極のどちらから何が発生するのかなど、細かなことまで覚えておく。



コメント(承認された場合のみ表示されます)
[…] 分解について・・・→【分解】← 酸化について・・・→【酸化と燃焼】← […]
[…] (中2で学習済み。詳しくは→【分解】←を参考に。) […]